Sécurité de la TEP/TDM et de la tomodensitométrie dans le diagnostic du cancer : comment calculer la dose de rayonnement et réduire le risque
Le contenu partagé ici est un résumé de l’article, pour l’article complet : visitez la section physique de la santé
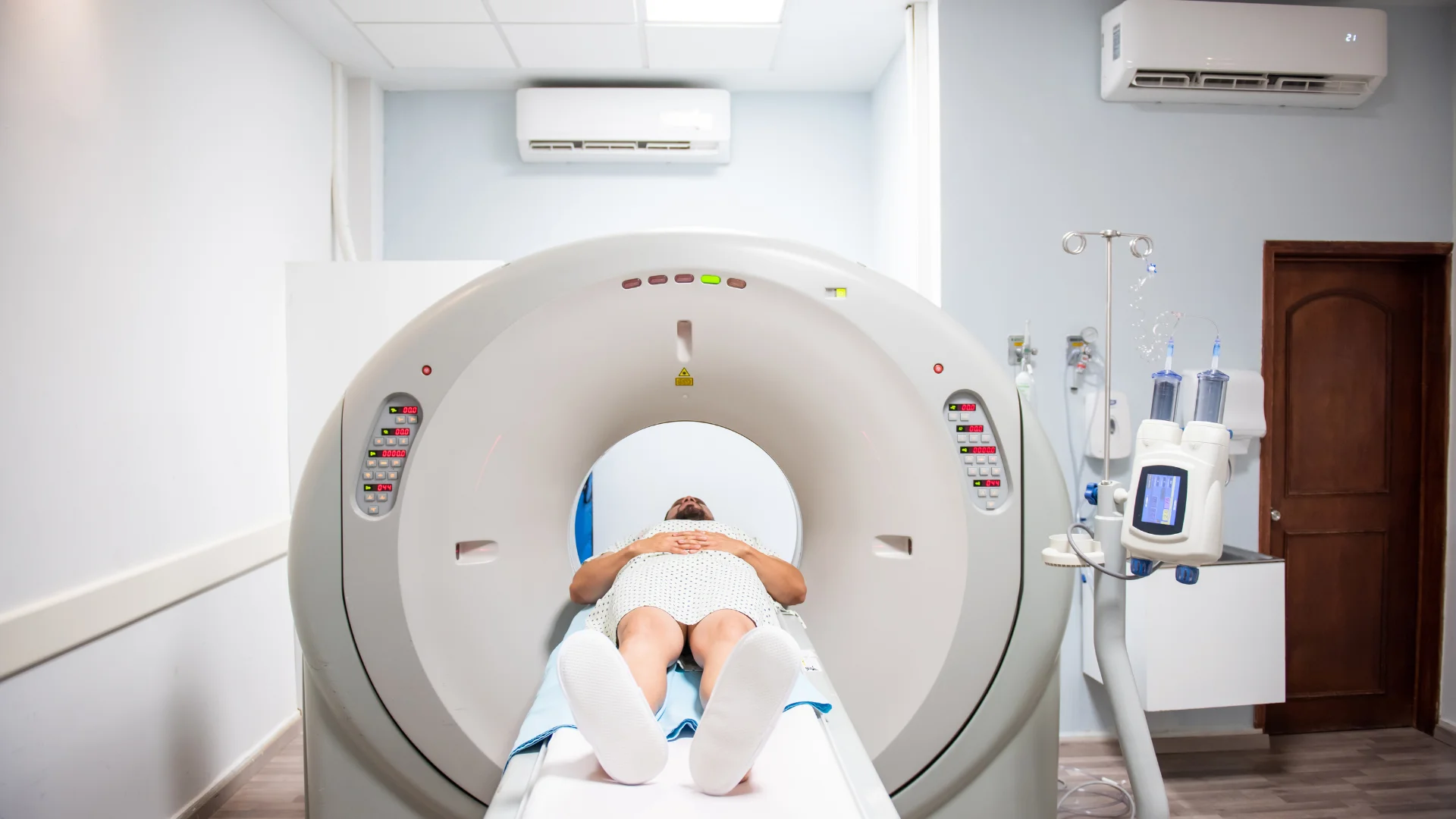
Le monde médical moderne repousse les limites avec des technologies qui changent radicalement les maladies, en particulier le processus de diagnostic du cancer . À l’apogée de cette avancée se trouvent les tomodensitogrammes par émission de positons et la tomodensitométrie (TEP/TDM), qui combinent des informations fonctionnelles au niveau cellulaire avec des détails anatomiques.
Ce puissant outil de diagnostic du cancer offre aux médecins des informations essentielles qui montrent où se trouve la tumeur et à quel point elle est active. Cependant, ce processus entraîne inévitablement une exposition aux rayonnements. Transformer ce risque invisible en données concrètes est l’une des responsabilités éthiques les plus importantes des scientifiques.
Cette responsabilité consiste à mesurer avec précision le rayonnement auquel le patient est exposé à l’aide de méthodes sophistiquées de calcul de dose efficaces par TEP/TDM .
Objet de l’étude : Cette analyse complète est basée sur les résultats d’une étude scientifique menée sur les données de 305 patients en oncologie au département de médecine nucléaire de l’Université de Yeditepe. L’objectif est de révéler l’impact critique des différents logiciels utilisés sur les prédictions de dose.
L’outil essentiel dans le diagnostic du cancer : qu’est-ce que la TEP/TDM ?
Lorsqu’un patient se rend à l’hôpital pour un diagnostic de cancer ou un suivi de traitement, les médecins veulent connaître non seulement la taille de la tumeur, mais aussi à quel point cette tumeur est « active ». C’est là que la TEP/TDM fait la différence. Ce balayage combine deux modalités d’imagerie différentes en une seule image haute résolution :
- TEP (tomographie par émission de positons) : fournit des informations fonctionnelles .
- Grâce au produit radiopharmaceutique injecté dans le patient, les activités métaboliques de l’organisme sont surveillées.
- Les traceurs comme le 18F-FDG suivent les cellules cancéreuses qui consomment de grandes quantités de sucre, montrant à quelle vitesse la tumeur se développe sous forme de points lumineux.
- TDM (tomodensitométrie) : Fournit des informations anatomiques .
- La tomodensitométrie, également connue sous le nom de tomographie, crée une cartographie structurelle détaillée des organes, des os et des tissus à l’aide de rayons X.
La combinaison de ces deux images fournit aux médecins une carte complète qui montre à la fois l’emplacement exact (tomographie) et l’activité cellulaire (TEP) de la zone cancéreuse.
Le concept central de la radioprotection : pourquoi mesure-t-on la dose efficace ?
Étant donné que les procédures de diagnostic médical augmentent l’exposition totale aux rayonnements des individus, la question de la radioprotection est devenue centrale pour les applications TEP/TDM . La dose efficace est l’unité de mesure de ce risque.
La dose efficace fait bien plus que simplement mesurer l’énergie des rayonnements entrant dans le corps :
- Il prend en compte le type de rayonnement : Il calcule séparément le rayonnement interne des produits radiopharmaceutiques et le rayonnement externe des rayons X de la tomographie.
- Calcule la sensibilité des organes : Il détermine le risque de radiations développant des lésions biologiques et un cancer sur chaque organe.
Ce risque est calculé à l’aide de facteurs de poids tissulaire déterminés par la Commission internationale de protection contre les radiations (CIPR). Par exemple, les tissus comme la moelle osseuse ou les poumons ont un facteur de poids plus élevé parce qu’ils présentent un risque plus élevé de cancer par rapport à d’autres tissus.
Formule de calcul de base : Cette étude scientifique recueille des doses de TEP et de TDM pour calculer la dose efficace totale : EDTtotal=EDPET+EDCT
Cartographie du rayonnement interne : doses critiques pour les organes
Dès que le produit radiopharmaceutique est injecté dans le patient, il commence un voyage à travers le corps. Ce parcours est suivi par le
- 18F-FDG (traceur de glucose) :
- Il cible les tissus à forte consommation d’énergie (métaboliquement actifs) de l’organisme.
- Organes recevant la dose la plus élevée : La paroi du cœur et la paroi de la vessie. (Ex : paroi cardiaque 0,067 mGy/MBq chez la femme)
- 68Ga-PSMA (traceur du cancer de la prostate) :
- Il est conçu pour cibler les cellules de diagnostic du cancer de la prostate et est essentiellement excrété par les reins.
- L’organe le plus critique : Reins. Il a reçu la dose absorbée la plus élevée (0,184 mGy/MBq).
Ces données détaillées montrent que chaque médicament présente des risques différents pour différents organes et dans quelle mesure le processus de calcul de la dose efficace doit être spécifique au médicament.
Modèles humains virtuels : la différence entre OLINDA et le logiciel IDAC
Un logiciel spécialisé utilisant la méthodologie MIRD est nécessaire pour calculer la dose de rayonnement avec précision. Ces logiciels utilisent des modèles humains virtuels, également appelés fantômes , pour calculer le transfert du rayonnement d’un organe à un autre.
| Nom du logiciel | Type fantôme (modèle humain virtuel) | La différence critique | Tendance des résultats |
| OLINDA/EXM | Fantôme mathématique (géométrie simplifiée) | Les organes sont représentés par des formes géométriques simples. | Il a donné l’estimation de la dose la plus élevée. |
| Dose IDAC 2.1 | Voxel Phantom (modèle réaliste 3D) | Il utilise une modélisation 3D basée sur des données de tomodensitométrie (CT) de patients réels. | Il a donné l’estimation de dose la plus basse et la plus récente. |
Qu’est-ce que Voxel Phantom ? Il tire son nom de « voxel », qui signifie « pixel de volume ». Ces modèles 3D représentent la forme et la position des organes avec une plus grande précision anatomique par rapport aux anciens modèles simplifiés. Cette approche moderne a rendu les calculs plus réalistes.
Champ de bataille du calcul : différences frappantes dans les estimations de dose
Malheureusement, les logiciels qui prédisent le risque de radiation d’un patient ne donnent pas toujours le même résultat. La constatation scientifique la plus importante de l’étude est qu’il existe des différences statistiquement significatives (P<0,001) dans les résultats du calcul de la dose efficace en fonction du programme informatique utilisé et des références scientifiques (CIPR) sur lesquelles il est basé. Ces différences montrent que les anciennes méthodes de prévision ne reflètent pas fidèlement le niveau de risque actuel.
Dose efficace de TEP pour le protocole 18F-FDG : 9,96 mSv ou 6,28 mSv ?
Dans les scans avec le 18F-FDG, le traqueur de diagnostic de cancer largement utilisé, la distinction entre les résultats du calcul de la dose efficace TEP est vraiment remarquable :
- Approche héritée (OLINDA/EXM – ICRP 60) : À l’aide de fantômes mathématiques (modèle humain virtuel simplifié), ce logiciel a donné l’estimation la plus élevée, calculant la dose à 9,96 mSv.
- Approche actuelle (IDAC-Dose 2.1 – CIPR 103) : Ce logiciel actuel, qui utilise des fantômes de voxels réalistes (modèle humain virtuel 3D), a estimé la dose à 6,28 mSv et a donné la valeur la plus basse et la plus précise .
Pourquoi y a-t-il une grande différence ?
Cette différence critique de 3,68 mSv entre l’estimation la plus élevée et l’estimation la plus basse n’est pas due à une erreur, mais à l’avancement de la science. Le nouveau logiciel utilise deux mises à jour clés :
- Facteurs de poids des tissus : Les facteurs de poids des tissus mis à jour de la CIPR 103 évaluent le risque de radiation des organes de manière plus réaliste.
- Géométrie du fantôme Voxel : La géométrie fantôme voxelle, basée sur des données de tomographie de patients réels, calcule le transfert d’énergie avec plus de précision.
Points essentiels à retenir : Cela prouve concrètement que les logiciels plus anciens ont tendance à surestimer le risque de cancer d’un patient pour la même quantité de rayonnement.
68Comparaison de la dose efficace de TEP pour le protocole Ga-PSMA
Cette tendance à la baisse significative s’est poursuivie dans le protocole 68Ga-PSMA, le traceur utilisé pour le diagnostic du cancer de la prostate :
- Estimation la plus haute (OLINDA/EXM – ICRP 60) : Calculée comme suit : 3,65 mSv .
- Estimation la plus basse (dose IDAC 2,1 – CIPR 103) : Estimation la plus récente et la plus basse ( 1,83±0,27 mSv .
Ces résultats prouvent que les résultats du calcul de la dose efficace varient considérablement en fonction du modèle biocinétique sous-jacent (distribution du médicament radioactif dans le corps), du type de fantôme (modèle humain virtuel) et de l’actualité des références de la CIPR dans le logiciel utilisé. Sur la base de modèles plus anciens dans les deux protocoles, OLINDA/EXM a toujours donné les estimations de dose les plus élevées.
L’objectif principal de la sécurité : la tomographie (TDM) et l’atténuation des risques
La constatation la plus importante de l’étude en termes de radioprotection dans le diagnostic du cancerest peut-être que la majeure partie du rayonnement total exposé aux patients provient de la composante tomographie (TDM).
| Protocole | Contribution de la dose de tomodensitométrie (TDM) à la dose totale | Dose efficace moyenne de tomodensitométrie |
| 18F-FDG TE/TDM | Environ 75,6 % | 19.05±5.89 mSv |
| 68Ga-PSMA TEP/TDM | Environ 92 % | 20.17±5.87 mSv |
Principal point à retenir : Dans les scintigraphies 68Ga-PSMA, la quasi-totalité (92 %) de la dose totale provient d’une tomodensitométrie (TDM). Cela suggère que les stratégies de radioprotection devraient être largement axées sur l’optimisation des protocoles de tomodensitométrie.
Organes les plus touchés par l’exposition à la tomodensitométrie (séquentiel) :
- Poumons
- Estomac
- Côlon
- Moelle osseuse rouge
- Gonates
Principe de sécurité clinique : Les cliniciens doivent toujours appliquer le principe ALARA (As Low As Reasonably Achievable) pour réduire l’exposition aux rayonnements. Cela nécessite l’utilisation de techniques de tomodensitométrie à faible dose.
Conclusion : Efficacité scientifique et responsabilité éthique
Cette étude a prouvé que les outils de calcul de dose efficaces utilisés dans les applications TEP/TDM présentent des différences dans leur capacité à prédire avec précision le risque auquel les patients sont exposés lors du diagnostic de cancer.
- Le logiciel le plus récent, IDAC-Dose 2.1, fournit les estimations de dose efficace de TEP les plus basses et les plus réalistes.
- Le fait que la majorité de la dose totale de rayonnement provienne de la composante tomographie (TDM) confirme que l’optimisation continue des protocoles de TDM est l’étape la plus critique en termes de radioprotection .
Le « calcul de la dose efficace PET/CT » n’est pas seulement une valeur scientifique complexe, mais aussi un engagement en faveur de la sécurité des patients dans le processus de diagnostic du cancer de la médecine moderne.
Pensez-vous que l’intelligence artificielle et l’apprentissage automatique seront en mesure de porter les futurs systèmes de calcul de dose efficaces à un point où ils pourront faire des prédictions de dose précises à cent pour cent à l’aide de modèles biocinétiques individualisés spécifiques à la biologie unique de chaque patient ? Ce voyage scientifique et éthique sera la prochaine étape passionnante de la quête qui allie technologie et santé humaine.